배경 및 연구 설계
Retatrutide(LY3437943)는 활성화하는 새로운 단일 펩타이드 약물입니다.세 개의 수용체가 동시에: GIP, GLP-1, 그리고 글루카곤. 당뇨병이 없는 비만 환자에서 그 효능과 안전성을 평가하기 위해, 제2상 무작위 배정, 이중맹검, 위약대조 임상시험(NCT04881760)이 수행되었습니다. 총참가자 338명BMI ≥30 또는 ≥27이고 체중 관련 합병증이 하나 이상 있는 환자들은 위약 또는 리타트루티드(1mg, 4mg을 2회 적정 일정으로, 8mg을 2회 적정 일정으로 또는 12mg)를 48주 동안 주 1회 피하 주사로 투여받도록 무작위 배정되었습니다.1차 종료점24주차 체중 변화율을 기준으로 하였고, 2차 종료점으로는 48주차 체중 변화와 범주별 체중 감소 임계값(≥5%, ≥10%, ≥15%)을 포함하였습니다.
주요 결과
-
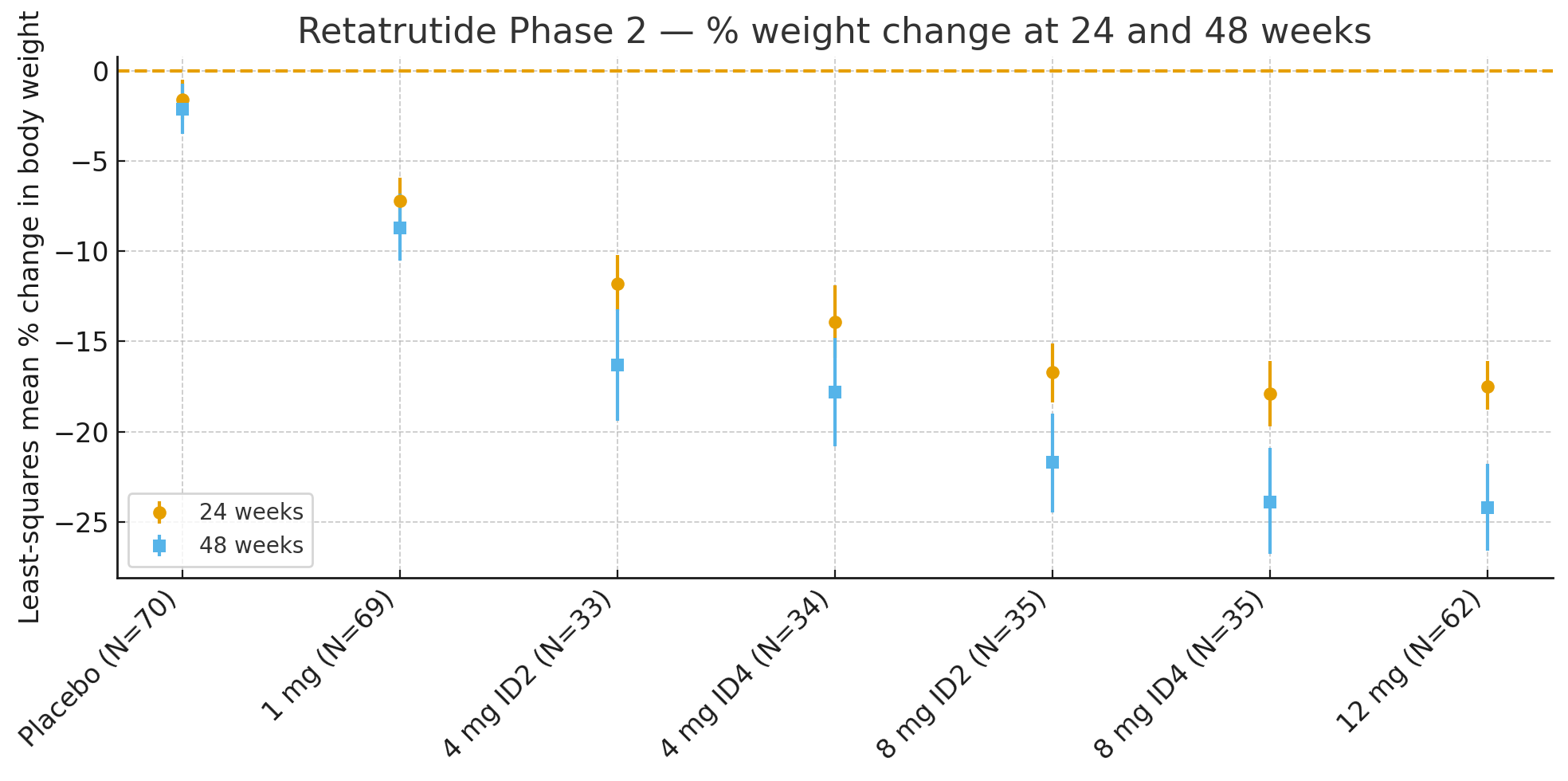
24주: 기준선에 대한 체중의 최소 제곱 평균 변화율은 다음과 같습니다.
-
위약: -1.6%
-
1mg: -7.2%
-
4mg(복합): -12.9%
-
8mg(복합): -17.3%
-
12mg: -17.5%
-
-
48주: 체중 변화율은
-
위약: -2.1%
-
1mg: -8.7%
-
4mg(복합): -17.1%
-
8mg(복합): -22.8%
-
12mg: -24.2%
-
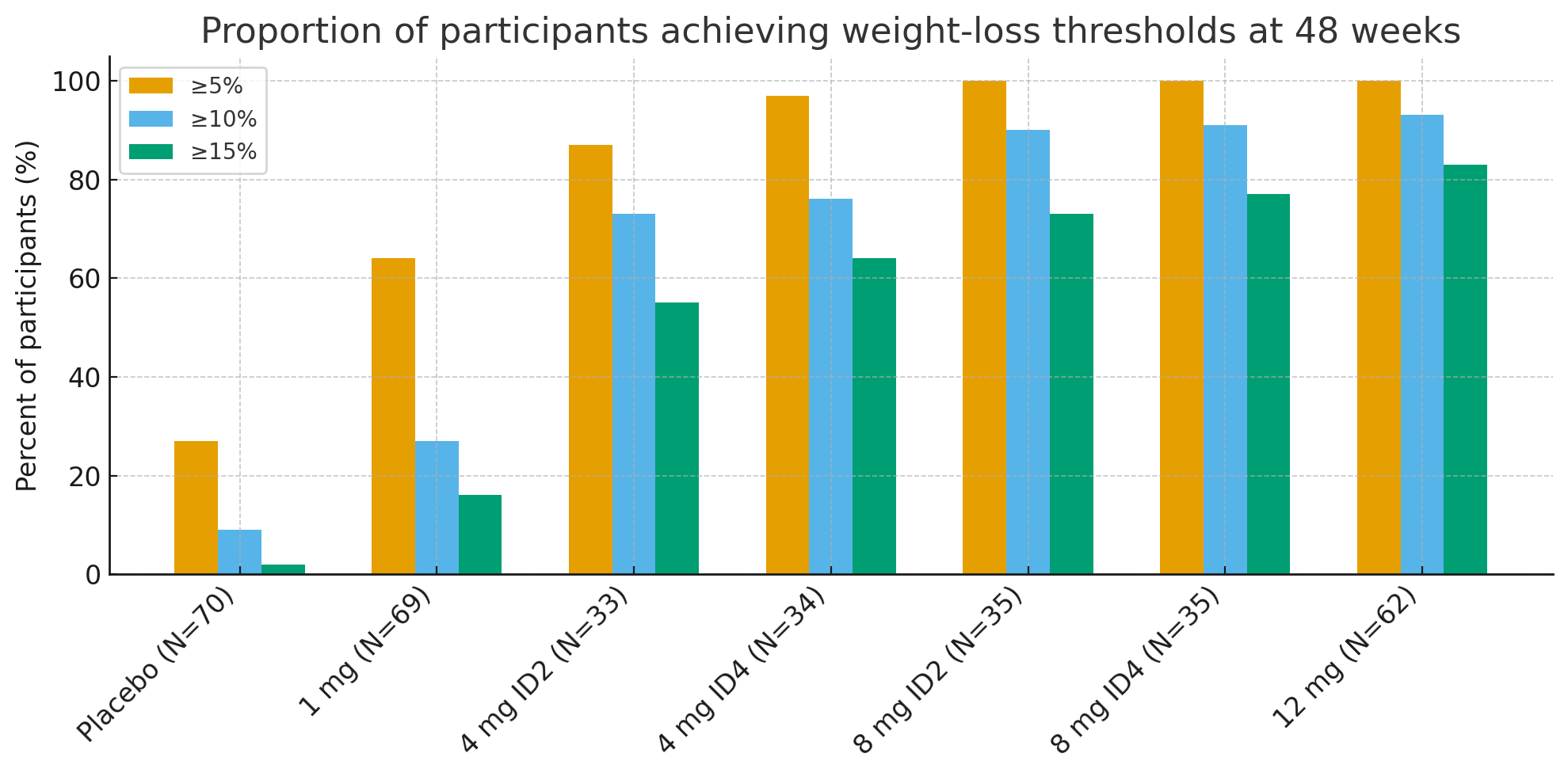
48주차에 임상적으로 의미 있는 체중 감량 한계점을 달성한 참가자의 비율이 놀라웠습니다.
-
≥5% 체중 감소: 위약군 27% 대비 활성군 92~100%
-
≥10%: 위약군 9% 대비 활성군 73–93%
-
≥15%: 위약군 2% 대비 활성군 55–83%
12mg 그룹에서는 최대참가자의 26%가 기준 체중의 30% 이상을 감량했습니다., 비만 수술과 비슷한 규모의 체중 감량이 가능합니다.
안전
가장 흔한 이상반응은 위장관계(메스꺼움, 구토, 설사)였으며, 일반적으로 경증에서 중등도였고 용량과 관련이 있었습니다. 초기 용량을 낮추었을 때(2mg 적정) 이러한 이상반응이 감소했습니다. 용량과 관련된 심박수 증가가 관찰되었으며, 24주차에 최고치를 기록한 후 감소했습니다. 투약 중단율은 활성군 전체에서 6~16%로 위약군보다 다소 높았습니다.
결론
당뇨병이 없는 비만 성인의 경우 48주 동안 매주 피하 주사로 리타트루티드를 투여하면체중의 상당한 용량 의존적 감소(최고 용량에서 최대 ~24%의 평균 손실) 심장대사 지표의 개선과 함께 나타났습니다. 위장관 부작용은 빈번했지만 용량 조절을 통해 관리 가능했습니다. 이러한 2상 결과는 리타트루티드가 비만에 대한 새로운 치료적 기준을 제시할 수 있음을 시사하며, 향후 더 큰 규모의 장기 3상 임상시험을 통해 확인될 예정입니다.
게시 시간: 2025년 9월 28일