2021년 8월 24일, Cara Therapeutics와 사업 파트너 Vifor Pharma는 최초의 카파 오피오이드 수용체 작용제인 디펠리케팔린(KORSUVA™)이 만성 신장 질환(CKD) 환자(혈액 투석 치료로 인한 중등도/중증 가려움증 양성)의 치료제로 FDA의 승인을 받았다고 발표했습니다. KORSUVA™는 2022년 1분기에 출시될 예정입니다. Cara와 Vifor는 미국에서 KORSUVA™의 상용화를 위한 독점 라이선스 계약을 체결하고 Fresenius Medical에 KORSUVA™를 판매하기로 합의했습니다. Cara와 Vifor는 Fresenius Medical을 제외한 다른 회사의 매출 수익에서 각각 60%와 40%의 이익 지분을 가지고 있으며, Fresenius Medical의 매출 수익에서 각각 50%의 이익 지분을 가지고 있습니다.
만성신장질환(CKD) 관련 가려움증(CKD-aP)은 투석을 받는 만성신장질환(CKD) 환자에게 높은 빈도와 강도로 발생하는 전신성 가려움증입니다. 가려움증은 투석을 받는 환자의 약 60~70%에서 발생하며, 이 중 30~40%는 중등도/중증 가려움증을 앓고 있습니다. 이는 삶의 질(예: 수면의 질 저하)에 심각한 영향을 미치고 우울증과 관련이 있습니다. 이전에는 만성신장질환 관련 가려움증에 효과적인 치료법이 없었으며, 디펠리케팔린의 승인은 이러한 막대한 의료적 필요성 격차를 해소하는 데 도움이 됩니다. 이 승인은 NDA 제출에 포함된 두 가지 주요 3상 임상 시험, 즉 미국과 전 세계에서 진행된 KALM-1 및 KALM-2 시험의 긍정적인 데이터와 KORSUVA™가 내약성이 우수함을 입증하는 32개의 추가 임상 연구의 긍정적인 데이터를 기반으로 합니다.
얼마 전, 일본에서 디펠리케팔린의 임상 연구에서 좋은 소식이 나왔습니다. 2022년 1월 10일, Cara는 파트너사인 Maruishi Pharma와 Kissey Pharma가 디펠리케팔린 주사제가 일본에서 혈액투석 환자의 가려움증 치료에 사용된다는 것을 확인했다고 발표했습니다. 3상 임상 시험 1차 평가 기준이 충족되었습니다. 178명의 환자가 6주 동안 디펠리케팔린 또는 위약을 투여받고 52주간 공개 연장 연구에 참여했습니다. 1차 평가 기준(가려움증 수치 평가 척도 점수의 변화)과 2차 평가 기준(시라토리 중증도 척도에서 가려움증 점수의 변화)은 위약군과 비교하여 디펠리케팔린 군에서 기준선에서 유의미하게 개선되었으며 내약성이 양호했습니다.
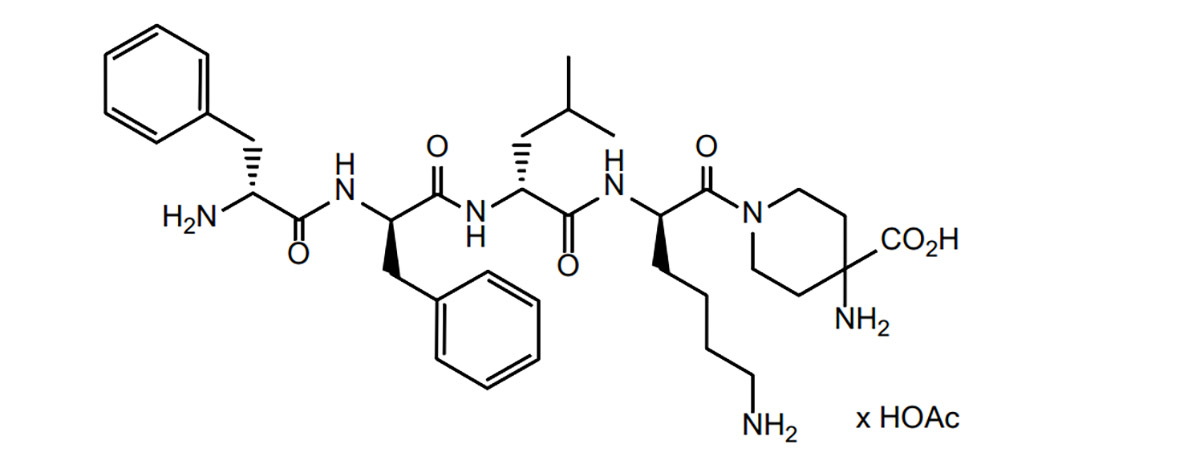
디펠리케팔린은 오피오이드 펩타이드의 한 종류입니다. 펩타이드 연구소는 이를 바탕으로 오피오이드 펩타이드 관련 문헌을 연구하고, 약물 개발 과정에서 오피오이드 펩타이드의 어려움과 전략, 그리고 현재 약물 개발 현황을 정리했습니다.
게시 시간: 2022년 2월 17일